Soolade keemilised omadused
Lõpetanud Egorova Yu.V., MKOU 4. Keskkooli keemia- ja bioloogiaõpetaja

- Esitage soolade kui elektrolüütide klassi mõiste.
- Mõelge klassifikatsioonile koostise järgi.
- Iseloomusta soolade omadusi ioonkontseptsioonide valguses.

soolad – kompleksained, mis koosnevad metalliioonidest ja happejäägist.
Soolad (terminist TED ) - Need on elektrolüüdid, mis dissotsieeruvad metalli katiooniks ja happejäägi aniooniks.

"Surnumere vesi"
Na 2 NII 4 - naatriumsulfaat
NaCl - naatriumkloriid
MgCl 2 - magneesiumkloriid
KBr - kaaliumbromiid

Soolade klassifikatsioon
Põhiline
Keskmine
Hapu

Vase soolad
Permanganaadid

1. harjutus
Uus raudpaak, milles valmistati taimede pritsimiseks vasksulfaadi lahust, lekkis. Selgitage paagi seinte hävimise põhjust.

Vihje
- Ma tean juba pikka aega
Ja mul on nõudlus.
Pange mind lahusesse -
Vasksulfaadis.
Ma tahan soola vahetada.
Noh, tulge välja, kui soovite.
Hämmastav hetk!
Lahendus sai teistsuguseks.
Ma nihutan elemendi välja
Vaidlusse laskumata.
Vaata mind, vasta:
Mis on mulle sisse saanud?

Koostoime metallidega
SOOL + METAL → UUS SOOL + UUS METAL
iga eelnev metall tõrjub soolalahusest välja vähemaktiivse metalli
Mg+ Fe Cl ₂ = MgCl2 + Fe ↓

Koostoime sooladega
sool1 + sool2= sool3↓+ sool4
Cu(NO ₃ ) ₂ + K₂S = 2KNO₃ + CuS↓

2. ülesanne
Mõnes linnas hävivad happevihmade tõttu arhitektuurimälestised. Kas neid saab päästa?

Vihje
Maa peal elab kolm venda Carbonate perekonnast.
Vanem vend on ilus marmor,
Kuulsusrikas Karara nimel,
Ta on suurepärane arhitekt
Ehitatud Rooma ja Parthenon.
Kõik teavad lubjakivi,
Sellepärast on see nii nime saanud.
Oma töö poolest kuulus
Maja taha maja ehitamine.
Nii võimekas kui ka võimekas
Noorem pehme vend on kriit.
Vaata, kuidas ta joonistab,
See ……….!

Koostoime hapetega
sool₁ + hape₁ → sool₂ + hape₂
CO ₂
K ₂ CO ₃ + 2 HCl = 2KCl + H ₂ CO ₃
H ₂ O

Koostoime leelistega
sool₁ + leelis = sool₂ + alus↓
AlCl ₃ + 3KOH = 3KCl + Al(OH)₃↓

3. ülesanne
Kuningas kutsub Amburi enda juurde,
Julge noormees
Ja annab talle juhiseid
Riiklik tähtsus.
Et ma saaksin uuesti rikkaks,
Vaja on baariumsulfaati.
Ma lasen sul öösel mõelda -
Jään hommikul reportaaži ootama!
Kui ei saa, kes on süüdi?
Ma pean sind hukkama.
Kirjutage oma nimi üles
Et hirmust mitte unustada.
Hankige baariumsulfaat võimalike meetodite abil.

D/Z Jne. 41, nt. 2,3,4 (kirjalik)

Slaid 1
Slaidi kirjeldus:
Slaid 2
Slaidi kirjeldus:
Slaid 3
Slaidi kirjeldus:
Müügimahu poolest on lauasool maitseainetest esikohal. Naatriumkloriid mitte ainult ei muuda toidu maitseomadusi, vaid omab ka suurt füsioloogilist tähtsust inimkehale: see on vere, lümfi, sapi ja raku protoplasma asendamatu komponent, toimib kudede ja rakkude osmootse rõhu peamise regulaatorina, reguleerib vee-soola ainevahetust ja happelisust - leelise tasakaal organismis on soolhappe tekke allikaks mao sekretsiooni protsessis jne.
Slaid 4
Slaidi kirjeldus:
Slaid 5
Slaidi kirjeldus:
Slaid 6
Slaidi kirjeldus:
Slaid 7
Slaidi kirjeldus:
Slaid 8
Slaidi kirjeldus:
Slaid 9
Slaidi kirjeldus:
Slaid 10
Slaidi kirjeldus:
Slaid 11
Slaidi kirjeldus:
Slaid 12
Slaidi kirjeldus:
Slaid 13
Slaidi kirjeldus:
Slaid 14
Slaidi kirjeldus:
See on aurutatud või jahvatatud sool, millele on meditsiinilistel ja profülaktilistel eesmärkidel lisatud kaaliumjodiidi (25 ± 5 x 10~4%). Kaaliumjodiidi stabiliseerimiseks lisatakse jodeeritud soolale lisaks lisasoolale ka naatriumtiosulfaati (25 ± 5 X 10 "%). Jodeeritud soolaga saab inimene umbes 200 mcg joodi päevas. See on aurutatud või jahvatatud sool, millele terapeutilisel ja profülaktilisel eesmärgil lisatakse kaaliumjodiidi (25 ± 5 X 10~4%). Kaaliumjodiidi stabiliseerimiseks lisatakse jodeeritud soolale naatriumtiosulfaati (25 ± 5 X 10 "%). ekstra soola. Jodeeritud soolaga saab inimene umbes 200 mcg joodi päevas.
Slaid 15
Slaidi kirjeldus:
Slaid 16
Slaidi kirjeldus:
Slaid 17
Slaidi kirjeldus:
Slaid 18
Slaidi kirjeldus:
Slaid 19
Slaidi kirjeldus:
Slaid 20
Slaidi kirjeldus:
Slaid 21
Slaidi kirjeldus:
3. Lauasoolas on lubatud massifraktsioon (%, mitte rohkem): arseen - 1 x 10", plii - 0,20 x 10, kaadmium - 0,20 x 10, elavhõbe - 0,01 x 10, vask - 2 x 10. 3 Lauasoolas on lubatud massiosa (%, mitte rohkem): arseen - 1 x 10", plii - 0,20 x 10, kaadmium - 0,01 x 10, vask - 2 x 10. 4. Kokkuleppel tarbijaga võib soola paakumise vähendamiseks lisada sellele kaaliumferrotsüaniidi - mitte rohkem kui 1 x 10%. 5. Niiskuse massiosa jodeeritud soolas - mitte rohkem kui 0,7 ± 0,02%. Kui soolale lisada kaaliumjodiidi, on lubatud nõrk joodi lõhn. Ülejäänud jodeeritud soola näitajad on samad, mis tavalisel soolal.
1 slaid

2 slaidi
Kõigist looduslikest mineraalsooladest on kõige olulisem see, mida me lihtsalt nimetame A.E. Fersmaniks

3 slaidi

4 slaidi
Sõna "sool" pärineb ladinakeelsest sõnast "sal", mis pärineb kreekakeelsest sõnast "hals", mis tähendab "merd".

5 slaidi
Ladinakeelne sõna "salarium" ja ingliskeelne sõna "salary", mis tähendab "palk", "palk", on "soola" päritolu.

6 slaidi
Rooma sõduritele anti luba osta salt salarium argentum, millest pärineb ingliskeelne sõna salary.

7 slaidi
Mõnikord maksti Rooma sõduritele soolas, aga ka "soldo" - münt, palk, mille sõdurid said vastutasuks nende valmisoleku eest verd valada - siit tuli venekeelne sõna sõdur.

8 slaidi
Ka roomlased eelistasid rohelist soolamist, mille tulemusena sai ladinakeelne sõna soola osaks uuest sõnast salat.

Slaid 9
Vana-Kreeka luuletaja Homeros nimetas lauasoola "jumalikuks". Neil kaugetel aegadel hinnati seda kullast kõrgemalt. Sõjalised kokkupõrked toimusid soolalademete pärast ja soola puudus elanikkonna hulgas põhjustas "soolamässud". M.V Lomonosov kirjutas, et tema ajal võis nelja-viie plaadi eest orja osta. Paljud Kesk-Aafrika hõimud vahetaksid tassi kulla tassi soola vastu. 13. sajandi Hiinas valmistati münte kivisoolast.

10 slaidi
Lauasool on inimestele tuttav juba ammusest ajast ja selle nimi on paljudes keeltes sarnane. Paljud linnad, jõed ja järved on nime saanud soola järgi: Soligalitš, Solikamsk, Solvitšegorsk, Sol-Iletsk, Soltsõ, Usolje ja Usolje-Sibirskoje; jõed - Usolka ja Solyonaya ning paljud teised.

11 slaidi
Naatriumkloriid on keemiline ühend NaCl, vesinikkloriidhappe naatriumsool. Naatriumkloriidi leidub merevees märkimisväärses koguses, tekitades selle soolase maitse. Looduses esineb see mineraalhaliidi (kivisoola) kujul.

12 slaidi
kristallid Haliit on kivisool, kloriidide alamklassi mineraal, naatriumkloriidi (NaCl) kristalne vorm.

Slaid 13
Naatriumkloriid (mõõtkavas mudel) Naatriumkloriid (kuuli ja pulga mudel) Naatriumkloriidi kristallvõre NaCl

Slaid 14
Lauasool kristalliseerub kuubiku kujul. Kuub on korrapärane hulktahukas, oktaeedr, millel on 8 tippu, 12 serva ja 6 tahku. Lauasoola kristallvõre sõlmedes olevad naatriumioonid Na+ ja kloor Cl- määravad kristallide kuupkuju. Naatriumkloriidi kristallvõre nimetatakse ioonkristallvõreks.

15 slaidi

16 slaidi
Mineraalmuuseumides eksponeeritakse suuri lauasoola kristalle 100-kilone kristall.

Slaid 17

18 slaidi
1960. aastatel hakati lauasoola – naatriumkloriidi – nimetama "valgeks surmaks" ja see hirmuäratav nimi on põlvest põlve edasi kanduv tänaseni. See on ebaõiglane ja vale. Muidugi võib soola liigkasutamine kergesti rikkuda oma südame-veresoonkonna ja kuseteede süsteemi ning viia end varakult hauda. Kuid see kehtib mis tahes toote kuritarvitamise kohta.

Slaid 19
Sool on inimkeha oluline komponent. Sool toetab kõigi kudede ja elundite moodustavate rakkude normaalset tegevust. Soolhapet toodetakse maos olevast soolast, ilma milleta on toitu võimatu seedida. Täiskasvanu päevane lauasoola vajadus on 10 – 15 grammi.

20 slaidi
On ütlus: "Et inimest hästi tunda, peate temaga koos sööma kilo soola." Selgub, et seda saab teha veidi enam kui aastaga. Inimese normaalse toitumise soolavajadus on ju vähemalt 7 kilogrammi aastas.

21 slaidi
Ilma soolata on imetajate keha olemasolu võimatu. Kõik bioloogilised vedelikud – veri, higi, uriin, sülg, pisarad, röga – sisaldavad naatriumi- ja kloriidioone. Naatriumkloriidi põhiülesanne on säilitada osmootne rõhk ja konstantne vedeliku maht. Naatrium ja kloor osalevad ka seedimises (vesinikkloriidhappeta ei seedu maos olev toit).

22 slaidi
stimuleerib ainevahetust; stimuleerib juuste kasvu; annab elujõudu ja jõudu; on osa maomahlast (0,2% vesinikkloriidhappe kujul). Cl- TÄHELEPANU! Ilma vesinikkloriidhappeta toidu seedimise protsess praktiliselt peatub.

Slaid 23
Na+ naatriumioon on peamine rakuväline ioon; leidub veres ja lümfis; koos kaaliumiioonidega annab: 1. Rakumembraanide läbilaskvus erinevatele ainetele. 2. Impulsi juhtimine piki närvikiudu. 3. Reguleerib vererõhku organismis.

24 slaidi
Sool on organismile ülioluline. Miks? Sellele küsimusele vastamiseks pidage meeles, millest inimkeha koosneb? 70% vett. Ja sool reguleerib ja hoiab veetasakaalu kehas. Teisisõnu, soola eemaldamine on sama, mis hingamise kõrvaldamine. Kuid see viib ka järelduseni: liigne või ebapiisav soola kogus toidus rikub selle tasakaalu.

25 slaidi
Kõik on kogenud: pärast soolase toidu söömist tahad juua. Palju. Samal ajal eemaldatakse kehast vähe vedelikku. Ja kus te arvate, kus kõik joogid hoitakse? Rasvarakkudes. Nad küllastuvad vedelikuga ja suurenevad oluliselt. Seetõttu probleemsed piirkonnad sageli paisuvad. Liiga palju soola - vedelikupeetus - ainevahetushäired - stress südamele ja veresoontele, neeruprobleemid. Veelgi enam, ainevahetushäired ja soolase toidu söögiisu tõus kutsuvad taas esile kaalutõusu.

26 slaidi
Pidev toidu alasoolamine, vastupidi, viib selleni, et eritub rohkem vedelikku ja hakatakse intensiivselt erituma vajalikke mikroelemente (eelkõige kaltsiumi, mis on oluline tugevate luude, küünte ja juuste kiire kasvu ning ilu jaoks).
Erandiks on ammooniumisoolad, milles NH4+ osakesed, mitte metalliaatomid, on seotud happeliste jääkidega. Tüüpiliste soolade näited on toodud allpool. NaCl – naatriumkloriid, Na2SO4 – naatriumsulfaat, CaSO4 – kaltsiumsulfaat, CaCl2 – kaltsiumkloriid, (NH4)2SO4 – ammooniumsulfaat.

Soola valem on üles ehitatud, võttes arvesse metalli ja happejäägi valentsi. Peaaegu kõik soolad on ioonsed ühendid, seega võib öelda, et soolades on omavahel seotud metalliioonid ja happeliste jääkide ioonid: Na+Cl– – naatriumkloriid Ca2+SO42– – kaltsiumsulfaat jne.

Soolade nimetused koosnevad happejäägi nimetusest ja metalli nimetusest. Peamine asi nimes on happejääk. Millest happe sool Happejääk Jäägi valentsus Soolade nimetus Näited Lämmastik HNO 3 NO 3 I nitraadid Ca(NO 3) 2 kaltsiumnitraat Räni H 2 SiO 3 SiO 3 2 II silikaadid Na 2 SiO 3 naatriumsilikaat Väävel H 2 SO 4 SO 4 2 II sulfaadid PbSO 4 pliisulfaat kivisüsi H 2 CO 3 CO 3 2 II karbonaadid Na 2 CO 3 naatriumkarbonaat Fosfor H 3 PO 4 PO 4 3 III fosfaadid AlPO 4 alumiiniumfosfaat Tabeli ülemises osas on hapnikku sisaldav happeline jäägid ja alumine osa näitab hapnikuvabu jääke.

Vesinikbromiid HBr Br I bromiidid NaBr naatriumbromiid Vesinikjodiid HI I I jodiidid KI kaaliumjodiid Vesiniksulfiid H 2 S S 2 II sulfiidid FeS raud (II) sulfiid Vesinikkloriid HClCl I kloriidid vesinikfluoriid vesinikfluoriid vesinikfluor2 ammoonium NH 4 Cl Tabelis on näha, et hapnikku sisaldavate soolade nimed on lõpuga "at" ja hapnikuvabade soolade nimed on lõpuga "id". Mõnel juhul võib hapnikuga küllastunud soolade puhul kasutada lõppu "see". Näiteks Na2SO3 on naatriumsulfit. Seda tehakse väävelhappe (H 2 SO 4) ja väävelhappe (H 2 SO 3) soolade eristamiseks ning muudel sarnastel juhtudel.

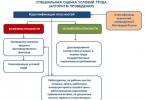
Soolade klassifikatsioon Sõltuvalt soola koostisest eristatakse: 1. Sööde - happes sisalduva vesiniku täieliku asendamise saadus metalliga. 2KOH + H 2 CO 3 = K 2 CO 3 + 2H 2 O kaaliumkarbonaat 2. Happeline – happes oleva vesiniku mittetäieliku asendamise saadus metalliga. NaOH + H 2 CO 3 = NaHCO 3 + H 2 O naatriumvesinikkarbonaat

3. Aluseline - OH rühmade mittetäieliku asendamise produkt - aluste happelise jäägiga. Mg(OH) 2 + HCl = MgOHCl + H 2 O magneesiumhüdroksükloriid 4. Topelt - koosneb erinevatest metalliaatomitest ja ühisest happejäägist. K 2 SO 4 + Al 2 (SO 4) 3 = 2KAl (SO 4) 2 alumiinium - kaaliumsulfaat














Munitsipaal riiklik õppeasutus Lütseum nr 11, Rossosh
Uurimine
"Maagiline sool"
Lõpetanud: Domnich Varvara 3- Klassis
Juht: Semeretšenko V.V.

EESMÄRK: UURIMISE SOOLA OMADUSTE, SELLE OMADUSTE JA OMADUSTE
Uuringu eesmärgid:
- uurida ajaloolist teavet soola kohta;
2. õppida tundma soola tähtsust elus
isik;
3. tundma ja kasutama
vajalikud ohutusmeetmed ja
kaitse katsete ajal;
4. viia läbi katseid soolaga;
5. analüüsida saadud
tulemused.

Hüpotees uuring:
Oletame, et sool pole mitte ainult inimese eluks vajalik aine, vaid ka huvitav materjal katseteks, vaatlusteks ja loovuseks.

Asjakohasus töö on leida lähedalt, vaatlemiseks ja uurimiseks ligipääsetavatest objektidest huvitavaid ja ebatavalisi asju.
ma valisin soola.
Sool on igal laual, igas kodus.
Minu vaatlusteks ja katseteks oli vaja ühte pakki lauasoola
maksab 14 rubla.

Sõna "sool" päritolu
mõnede kaasaegsete teadlaste arvates seostatakse seda Päikesega: Päikese iidne slaavi nimi on Solon.

Natuke ajalugu...
Venemaal, 16. sajandil, kuulsad vene ettevõtjad Stroganovs Suurimad sissetulekud said soola kaevandamisest. Stroganovs olid suurimad soolakaevurid. Nad elasid Permi piirkonnas. Just sool tegi tollal Permi piirkonna kuulsaks kogu Venemaal.
Sealt ja Uurali jalamilt saadeti soola Moskvasse, Kaasani, Nižni Novgorodi, Kalugasse ja isegi välismaale.

Meetodid soola ekstraheerimiseks.
Kivisool Neid kaevandatakse kolmel viisil: karjäärides ja kaevandustes, kui sool on sügavale maetud, ja maa-aluse lahustamise teel - kui kihid on õhukesed ja sageli aherainega kaetud. Lisaks ekstraheeritakse ja keedetakse ka looduslikke maa-aluseid soolvesi.
Ise istutav sool minu oma
järvedes.
Mereline (aurustamine) sool ekstraheeritakse kanalitega ühendatud basseinide süsteemi abil, millest vesi järk-järgult tühjendatakse. Igas basseinis ladestub üks aurustumismineraalidest, halvasti lahustuvatest kuni kergesti lahustuvateni.

Leib ja sool
Vana traditsiooni kohaselt tervitatakse Venemaal tähtsat külalist ikka veel leiva ja soolaga: ta peab leivatüki ära murdma, soolama ja ära sööma. See on hea soov, külalislahkuse väljendus. See iidne rituaal tähendab, et külaline on astunud sõbralikesse suhetesse ja on valmis koos sööma
tervitatud soolatäpiga,
valmis neid kõiki jagama
mured ja mured.

Sool rahvamärkides
Soolaga on seotud palju ebausku ja märke,
üks kuulsamaid:
Soola mahaloksumine on halb enne.
Palju-palju aastaid tagasi polnud soola
igas majas. Nad panid selle lauale
ainult kõige väärtuslikumatele külalistele.
Kui külaline kogemata või, mis veelgi hullem, selle meelega maha puistas, peeti seda lugupidamatuks võõrustajate vastu.
Siit tuli see märk:
kui soola maha puistate, tekib tüli.

Sool rahvakunstis
Vanasõnad
"Sool on kõige pea, ilma soolata on muru muru"
"Soola pole ja sõna pole"
“Laud on kõver ilma soolata”
MÕISTATUSED
Valge kivi mäest on alati laual.
Kes seda ei söö, see maitset ei tunne.
Nad ei söö mind üksi ja ilma minuta ei söö nad palju.


"Sööt" jää jaoks"
Järeldus: sool, olles jääle sattunud, sulatab veidi sellest väikese osa. 5-10 minuti jooksul lahustub sool vees ja jääpinnal olev puhas vesi külmub koos niidiga.

ujuv muna
Pandi toores muna purki
värske veega, see kohe
vajus põhja.
Teises pangas tõid nad tugeva
soolalahust, tilgutas selle sinna
meie muna. See hakkas hõljuma
pinnal. Sellesse purki
hakkas aeglaselt kallama
mage vesi. Muna on saanud
vajus alla, kuid ei uppunud.
See hõljus keskel
lahendus, aga eks näis
suur ja ümmargune.
Ja kui nad muna välja võtsid, oli see sama.
Järeldus: Sool suurendab vee tihedust.
Mida rohkem on vees soola, seda raskem on sellesse uppuda.

Mittekülmutav sool.
Järeldus: Soolane vesi ei muutu madalal temperatuuril jääks. Seda soola omadust kasutatakse talvel teedel.

Minu käsitöö soolast.

Järeldus
Praktiline tähtsus- meie tehtud katseid ja uuringuid saab kasutada ümbritseva maailma ja tehnoloogia tundides, koolivälises tegevuses ja klubitundides.
Uurimise käigus saime teada, et soola ajalugu ulatub aastatuhandete taha, et see oli kunagi luksuskaup ja selle tõttu algasid sõjad.
Saime teada, et enne, kui inimesed ei teadnud, kust see pärit on, kuidas seda saada, omistasid nad sellele maagilisi omadusi – sellepärast oli see nii kallis
Saime teada, et tänapäeva maailmas kasutatakse soola mitte ainult toiduainetööstuses, vaid ka paljudes muudes valdkondades ja sellel on lai valik rakendusi.
Olime veendunud, et kaasaegne maailm ei omista soolale “maagilisi” omadusi, vaid vajab seda vähem kui meie esivanemad.
Tegime praktilisi katseid ja õppisime tundma mõningaid soola omadusi.

Kirjandus:
1. Entsüklopeedia "Kõik kõige kohta." T. 2,6,8,11 M.: “Ajakirjandus”, 1995. a
2. Entsüklopeedia “Mis see on? Kes see?" Kirjastus "Pedagoogika", M., 2009.
3. Entsüklopeedia “Ma tunnen maailma”, M.:AST “Astrel”, 2009
4. Yu.R. Vasiliev “Meelelahutuslik looduslugu”, M., “Omena”, 1997
Interneti ressursid:
1. "Meelelahutuslikud katsed köögis" - http://adalin.mospsy.ru/l_01_00/l_01_10m.shtm
2. “Meistrite riik. sool" - http://stranamasterov.ru/taxonomy/term/1706

TÄNAN TÄHELEPANU EEST!